安全性情報管理(GVP)サービス
フルサポートも一部委託も、迅速・確実に支援
医薬品・医療機器の臨床試験と製造販売後に発生する、国内外の安全性情報の入力や評価案作成などを支援します。安全性情報管理業務では、受付、入力およびQCチェックから翻訳、症例報告書案作成に至るまで、フルサポートのほか一部業務受託も可能です。
状況に応じてオンサイト(お客様社内常駐)、オフサイト(当社事業所内)のいずれのロケーションにも柔軟に対応します。
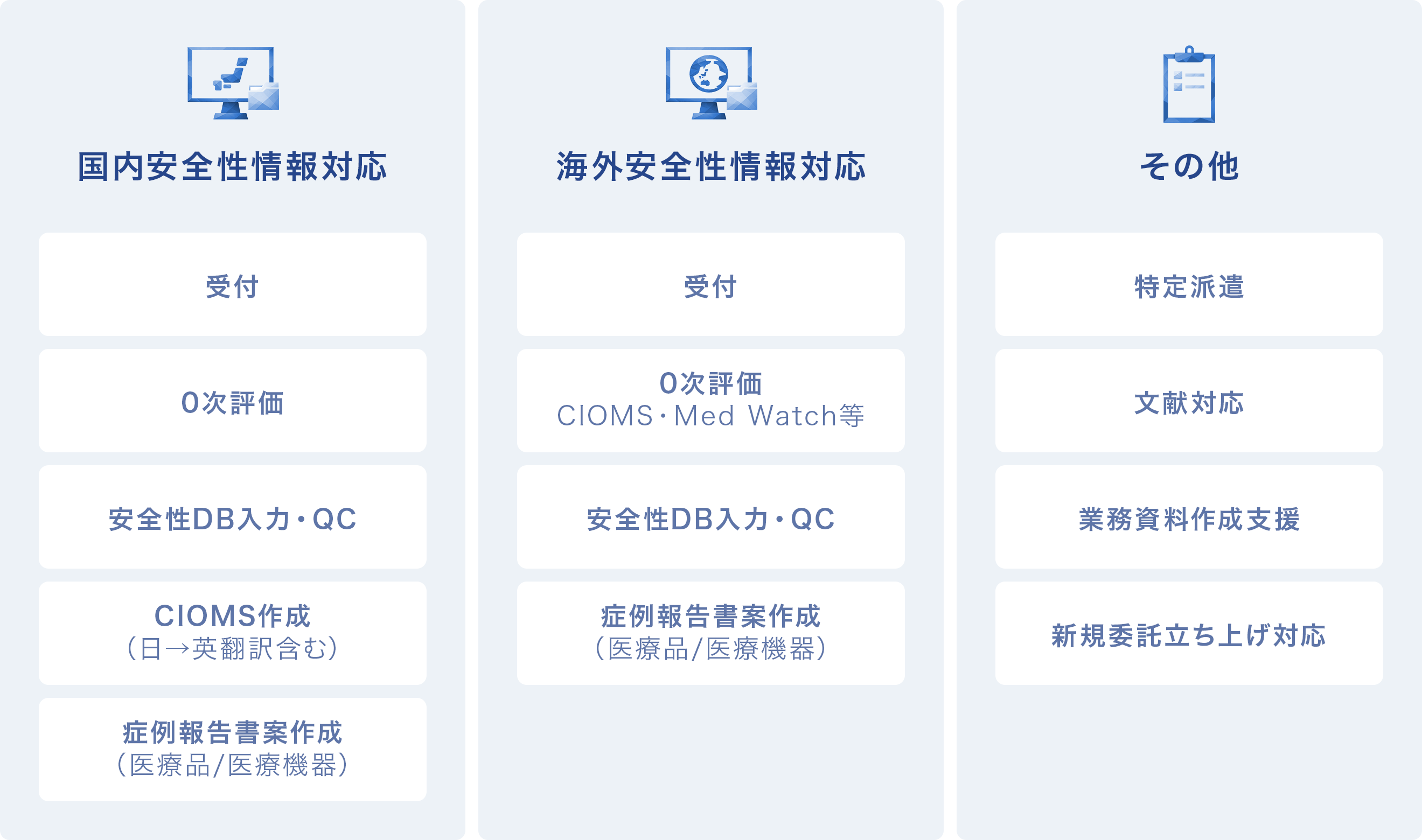
 国内安全性情報対応
国内安全性情報対応
安全性情報の受付から安全性データベースへの入力、評価(案)の作成、英訳を含むCIOMSフォーム作成まで、シームレスに支援いたします。
 海外安全性情報対応
海外安全性情報対応
国内安全性情報対応と同様に、語学力に長けたスタッフが、受付から評価(案)の作成、PMDAへの報告書作成まで一貫して支援するほか、海外提携先からの安全性情報収集や和訳も承ります。
 その他
その他
下記業務にも対応いたします。
継続的な業務のほか、一時的な業務支援も対応可能です。お気軽にご相談ください。
• 薬剤ごとの既知/未知事象の構築
• 文献情報のスクリーニングから評価(案)、報告書(案)作成
ArkMSの特長・強み
当社は、18年以上にわたり積み重ねてきた30件以上の受託実績とノウハウを活用し、安全性情報管理支援サービスを提供しています。


お客様に寄り添った柔軟なサービス提案
安全性情報管理業務経験者が、お客様の課題に同じ目線で向き合い、新規業務委託の立ち上げをはじめ、オンサイトまたはオフサイトでの支援や、一部業務のみの委託など、柔軟に対応いたします。


品質の維持・向上に向けた継続的な取り組み
当社では受託業務ごとに品質維持のための継続研修を行っています。
プロジェクトごとの課題と改善策、ノウハウなどを水平展開して高い品質を維持し、高精度なサービスを実現しています。





