臨床開発のサービス
豊富な実績・知見・先進性で、医薬品・医療機器等の治験・臨床開発を支援
フルサポートCROとして、治験における研究計画の立案からPMDA相談、事務局業務、モニタリング、データマネジメント・EDC構築/運用、統計解析、メディカルライティングをフルサポート、または各業務単位でのご依頼内容にも適宜対応いたします。
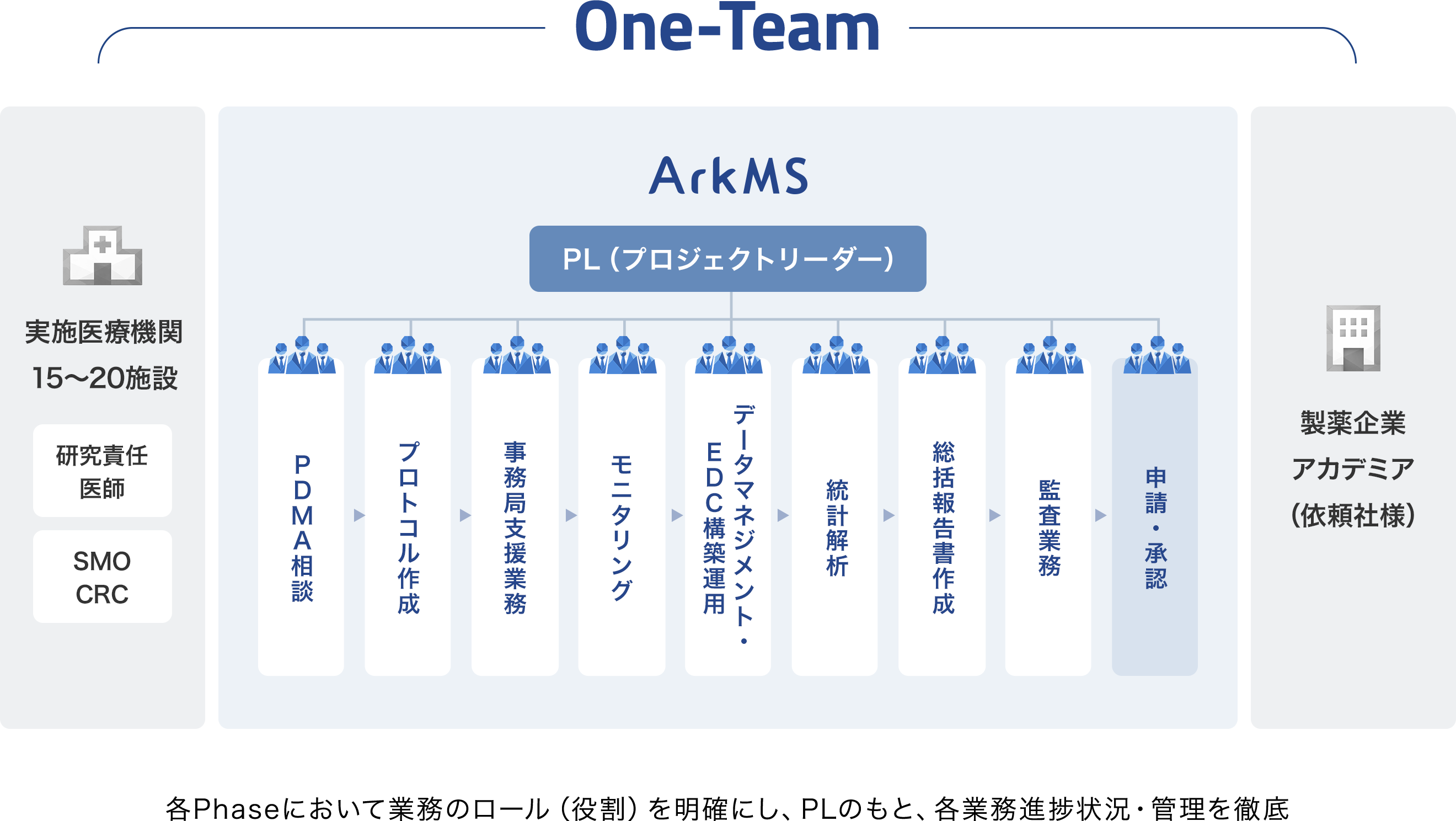
プロジェクト単位にて最適な責任者・担当者をアサインし“One-Team”体制にて実施・完遂
多様化を続ける臨床試験ニーズに対し、豊富な経験を持つメンバーが、効率性と品質の最適なバランスを実現する戦略を提案し、柔軟な開発推進支援を行います。
依頼者様を含めた“One-Team”体制にて各役割を明確にし、治験が初めてのスタートアップの企業様、医療機関・アカデミアの治験、医師主導治験の支援をパートナーとしてスピード感をもって伴走します。
 PMDA相談/プロトコル作成支援
PMDA相談/プロトコル作成支援
多岐にわたる経験から最適な臨床試験デザインを相談・協議し、規制やガイドラインを遵守したプロトコル案の提案や、全般相談・開発前相談から支援を行います。
<主な対応業務>
- 治験薬概要書
- プロトコル骨子案作成
- PMDA相談対応
 調整事務局支援業務(医師主導治験)
調整事務局支援業務(医師主導治験)
円滑な治験遂行のため、多施設対応の煩雑な実施医療機関の対応を含めた調整事務局業務を主導します。治験前の初期準備となる各種書類作成をはじめ、IRB(倫理審査委員会)対応、医療機関・医師との緊密な連携構築など幅広くサポートします。
<主な対応業務>
- 治験届
- 各種ドキュメント類/手順書の作成
- 同意説明文書作成
- 参加医療機関に対する業務支援
- 倫理審査・IRB対応
- キックオフミーティングの調整
- 終了手続き
 モニタリング業務
モニタリング業務
治験を熟知したプロジェクトマネージャーレベルのモニタリングチームが、試験全体のゴールを見据えて、データマネジメント担当や統計解析担当と連携し迅速かつ正確なモニタリングを実施します。また、医療機関との密なコミュニケーションを通じて、治験の円滑な進行をサポートし、患者様の安全確保を最優先に考えたモニタリングを実施します。
また、Risk-Based Approach to Monitoring(RBM)やDecentralized Clinical Trial(DCT)といった最新の手法にも対応可能。弊社が窓口となり、お客様のご要望に合わせ、協業会社様と共同で最適なモニタリングプランをご提案します。
<主な対応業務>
- 試験全体のプロジェクトマネジメント
- 施設選定/Feasibility調査
- 実施医療機関への依頼、契約手続き
- 治験薬交付、回収
- 症例管理、進捗管理
- 実施計画書(案)作成支援
- 直接閲覧、SDV
- 被験者同意説明資料(案)作成支援
- CRF回収、クリーニング
- 治験薬(機器/製品)概要書
- 終了手続き
 データマネジメント/EDC構築・運用業務
データマネジメント/EDC構築・運用業務
データマネジメントの専門家 (弊社データマネージャー) が、EDC構築~運用、データマネジメント業務を一貫して担当することで、認識の齟齬を最小限に抑え、高品質かつ効率的なデータ管理を実現します。
多様な治験の特性に合ったソリューションを提供し、仕様確定後約2か月~4か月でEDC構築から治験開始を実現します。ePRO連携によるデータ取得/管理方法の提案も可能です。
また、システム構築後も、軽微な変更や項目の追加などのご要望においては、柔軟に対応します。
<主な対応業務>
- データマネジメント業務手順書・計画書の作成・eCRFの作成・クエリ対応(ロジカルチェック・マニュアルチェック)
- 症例検討会資料の作成
- データベース設計・構築/入力システム作成
- EDCシステムのセットアップ
- システムバリデーションの実施
- データマネジメント業務報告書の作成
- CDISC標準(SDTM)のデータ作成支援
- データ入力・修正/コーディング
 統計解析業務
統計解析業務
多種多様な疾患領域における実績・学術的知識、高度なプログラミング(SAS)技術を有する生物統計の専門家が、解析計画立案から結果報告までを行います。追加解析や照会事項の発生時には、柔軟かつ迅速に対応します。
CDISC標準(SDTM・ADaM)対応において、データマネジメントと統計解析の専門チームが円滑に連携して対応します。
<主な対応業務>
- 統計解析手順書作成
- 統計解析計画書作成
- 解析用データセット作成、帳票作成、仕様書作成
- 解析プログラム作成
- 解析報告書作成
- CDISC標準(ADaM)
 総括報告書作成業務
総括報告書作成業務
熟練のメディカルライターを中心に、広範な専門知識を有するライターが、関連法規や各種ガイドラインを遵守し、書類を作成します。
承認申請資料として求められる品質を保持し、申請・承認プロセスの迅速な完了に貢献します。
<主な対応業務>
- 治験総括報告書(案)作成支援
- 治験結果の論文(案)作成支援
 監査
監査
臨床試験データやプロセスが、関連法規や各種ガイドラインをはじめ、実施計画書、標準業務手順書(SOP)などに適合していることを確認します。
弊社では、治験の信頼性を確保するため、依頼者様にご確認いただいた上で、協力会社または第三者機関による監査を実施し、客観的な視点を取り入れています。客観的かつ独立した視点から、潜在的なリスクを特定し、是正措置や改善策をご提案することで、適合性調査での指摘を最小限に抑え、承認申請まで迅速に進むようにサポートします。
<主な対応業務>
- 医薬品、医療機器の治験・臨床研究の監査
- 治験関連業務の社内監査
- 治験実施医療機関の監査
- ベンダーの監査・評価
- 治験審査委員会、倫理審査委員会の監査
受託実績
幅広い疾患領域、研究種別
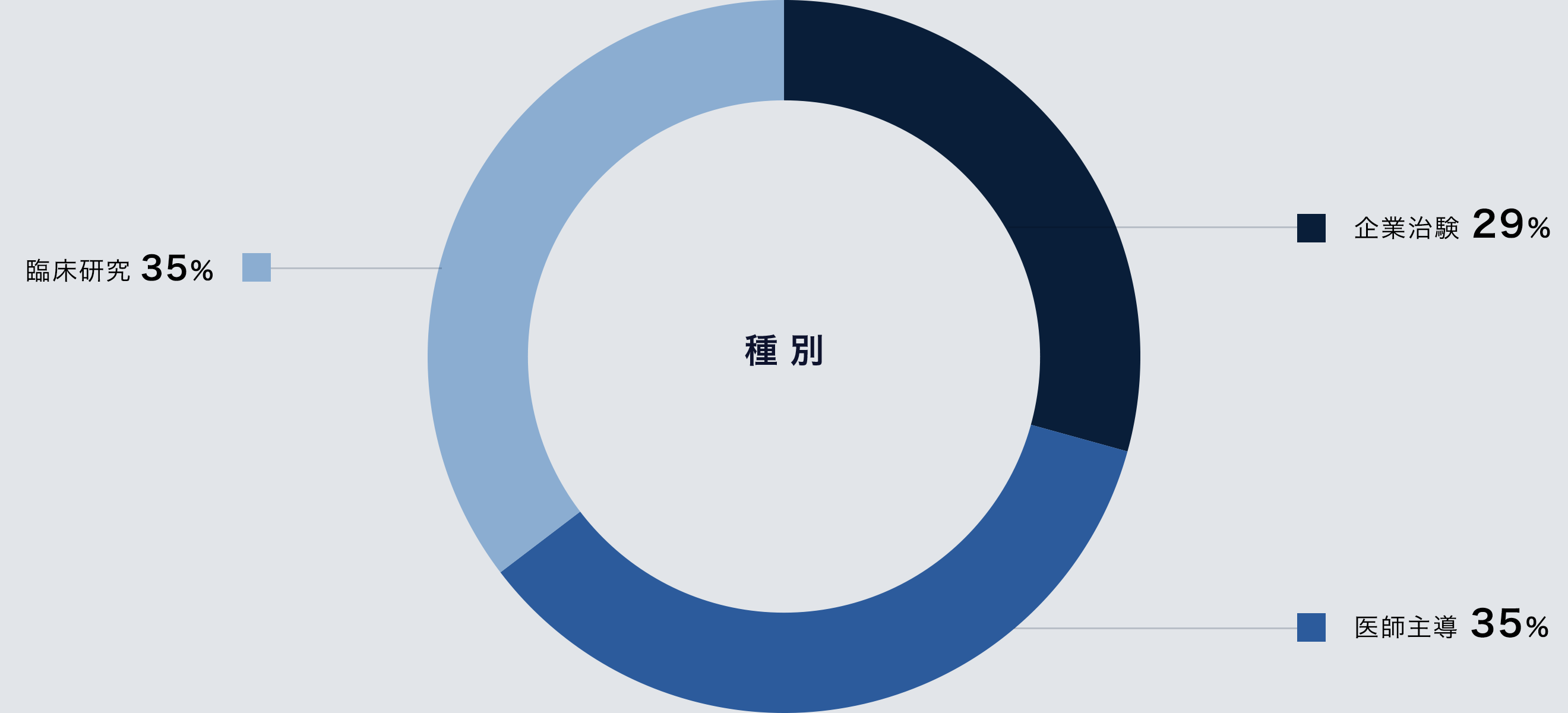
治験・研究種類別の割合
治験経験のある各業務責任者・担当者において効率的な企業治験・医師主導治験・特定臨床研究・観察研究を提案・実施いたします。
臨床研究においては、特定臨床研究、前向き・後向き観察研究、レジストリー研究、疫学研究など、さまざまな研究種別での実務経験があります。また、アカデミア支援として、医師主導治験や研究者主導の治験・研究も積極的に支援しています。
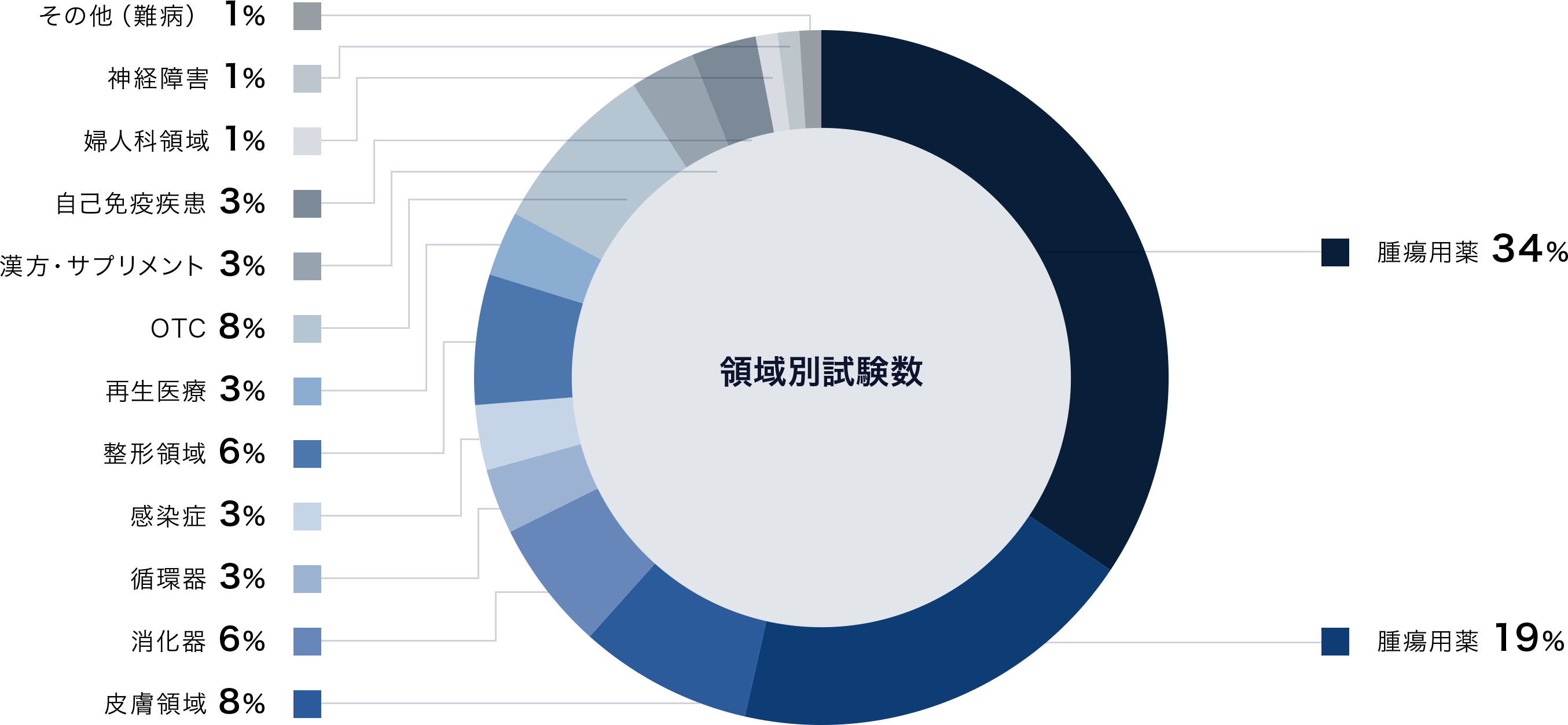
疾患領域
近年では、腫瘍領域・DTx(治療アプリ・診断プログラム医療機器)分野・医療機器・再生医療の領域、OTCなど、幅広い実績を積み上げています。
特にDTx分野にいち早く取り組み、医療機器領域の50%は治療用・診断用アプリなどのDTx関連試験です。国内2例目の治療用アプリを含め、2件の国内承認の支援を行いました。
実施事例
スタートアップ企業様のパートナーとして並走
DTx治験における成功事例
Case.01 治療用アプリ2件と診断プログラムの企業治験
1 課題相談
スタートアップ企業様のため、リソース不足かつ治験経験者が少数であり、限られた予算内で、PMDA相談対応~IRB~施設選定の初動からフルサポート支援を希望しました。
2 対応事例
社内の各業務責任者に治験経験者での実施体制を構築し、プロジェクトマネージャーを配置。クライアント様と一体となるOne-Team体制で実施。
スムーズなコミュニケーションにより進捗管理や課題解決が的確・迅速に図られました。
3 結果
適合性調査において大きな指摘なく承認申請対応へ移行しました。
後日、無事に保険償還・販売に至りました。
クライアントからの評価
監査や適合性調査において大きな指摘なく承認申請対応が完了し、無事に保険償還・販売となりました。
弊社担当者(PM)
依頼者様と同じ視点と意思を持って目標に向かって並走し、承認取得時には達成感を感じました。綿密な打ち合わせとCRA対応力向上により、治験成功へとつなげることができました。
医師主導治験・研究において多忙な医師・医療機関ご担当者様とともに円滑に対応
Case.02 医師主導治験・研究
1 課題相談
- 助成金、院内予算などに合わせて工数調整・効率化
- 院内のリソースが不足している業務パートにおいて、役割分担を明確にした個別業務支援
- 弊社への委託により、事務局機能を安定化した実施体制を構築
2 対応事例
- リスクベースでモニタリング計画を策定し、委託先のKPI・報告様式・逸脱時の是正手順まで定義
- 安全性情報の受付窓口から報告日のタイムライン管理(アラート)を整備
- CTN提出用資料作成支援と改訂履歴管理(版管理・承認フロー)など
3 結果
必須文書とSOPが揃い、治験開始前の準備作業が属人化せず再現可能な形に整理されました。
モニタリング所見・逸脱・データクエリの回転が改善し、品質(信頼性)とスピードが両立し、SAE等の初動と当局報告が標準化され、期限遅延・報告漏れリスクを低減できました。
文書改訂と記録保存の統制が効き、監査/調査対応での手戻りが無くなり、運用が安定しました。
医師・院内AROからのご評価
調整事務局で情報が一元管理されており、試験本数を重ねるごとに試験実施が円滑になってきています。
弊社担当者(PM)
AROご担当者様と調整しながら、各院内の状況を考慮し、知見を増やしながら進めています。











